Sono il pilastro della medicina moderna, molecole in grado di debellare malattie un tempo incurabili. Stiamo parlando dei farmaci, eredi dei rimedi naturali utilizzati fin dall’Antico Egitto e oggi prodotti su larga scala grazie all’industrializzazione, che ha reso possibile trattare un numero crescente di pazienti e sviluppare nuove molecole in laboratorio. Ma dopo aver svolto la loro funzione, queste sostanze non scompaiono: vengono eliminate dall’organismo e possono continuare a circolare nell’ambiente, con effetti che vanno ben oltre quelli terapeutici. Negli ultimi due decenni la spesa sanitaria globale è più che raddoppiata e, secondo lo United Nations Enviroment Programme (UNEP), oggi vengono somministrati circa 4.000 farmaci, un quarto dei quali circa finisce nelle acque di almeno 89 Paesi diversi, spesso senza alcun processo di trattamento. La farmacologia moderna si configura così anche come una fonte crescente di inquinamento ambientale su larga scala. Un progresso che ha un costo anche in termini di equità, concentrandosi nei Paesi ad alto reddito, che secondo l’Organizzazione mondiale della sanità assorbono circa l’80% della spesa sanitaria globale, mentre oltre metà della popolazione mondiale resta senza accesso ai servizi essenziali e un terzo non può permettersi i farmaci necessari (dati World Health Organization).
Eppure, circa il 70% dei farmaci deriva dalla biodiversità — dalla morfina al captopril — ma allo stesso tempo contribuisce alla sua pressione e al suo declino. Un paradosso che rischia di trasformarsi in un effetto domino: dal danno agli ecosistemi fino a ricadute dirette sulla salute umana.
Dal principio attivo all’effetto
«Il problema è legato all’uso terapeutico, alla produzione industriale, alla zootecnia e allo smaltimento, soprattutto se inappropriato», spiega Giovanna Paolone, professoressa all’Università di Verona e a capo del Gruppo di lavoro sull’impatto ambientale dei farmaci della Società Italiana di Farmacologia (SIF). «Il fenomeno è ampiamente documentato e in crescita, sebbene la distanza tra ciò che sappiamo e ciò che sarebbe necessario fare sia ancora tanta. Dai monitoraggi sistematici avviati in Europa, soprattutto dopo la Direttiva Quadro sulle Acque del 2000, sono state rilevate centinaia di molecole di farmaci e loro metaboliti nelle acque superficiali, nelle falde acquifere, nei suoli agricoli, nei sedimenti marini e persino nell’acqua potabile di molte città europee».
I primi effetti dei farmaci sull’ambiente furono documentati negli anni ’90, quando uno studio pubblicato su Chemistry and Ecology ha rilevato la femminilizzazione dei pesci a valle degli impianti di trattamento delle acque reflue, attribuita alla presenza di composti estrogenici, con conseguenze significative per la sopravvivenza di diverse specie. Non solo: come spiega ancora Paolone, «Farmaci come gli inibitori della ricaptazione della serotonina (SSRI) alterano il comportamento riproduttivo e predatorio di pesci e anfibi a concentrazioni ambientali realistiche, mentre alcuni pesci manifestano agitazione permanente dopo l’esposizione alla caffeina. Un altro esempio famoso è la strage, nel subcontinente indiano, degli avvoltoi che si nutrivano di carcasse di bovini trattati con diclofenac, altamente nefrotossico per loro, a cui viene fatta risalire la nascita dell’ecofarmacovigilanza», ovvero l’insieme delle attività di rilevazione, valutazione e prevenzione degli effetti negativi legati alla presenza dei prodotti farmaceutici nell’ambiente.
Un altro passaggio storico cruciale è segnato dalla pubblicazione di uno dei primi studi, agli inizi degli anni 2000, che correla le concentrazioni anomale di farmaci negli effluenti industriali alla resistenza antibiotica (AMR), con antibiotici come la ciprofloxacina che mostrano carichi pari a 45 kg al giorno (la quantità totale consumata in Svezia in cinque giorni!). «La resistenza agli antibiotici è accelerata dall’ambiente, poiché i batteri nei sedimenti fluviali e nei terreni agricoli fertilizzati con i fanghi di depurazione sono costantemente esposti a concentrazioni subterapeutiche di antibiotici: condizione ideale per la selezione e diffusione di geni di resistenza. Non è un caso che questa sia riconosciuta dall’Organizzazione mondiale della sanità come una delle vie di amplificazione dell’AMR».
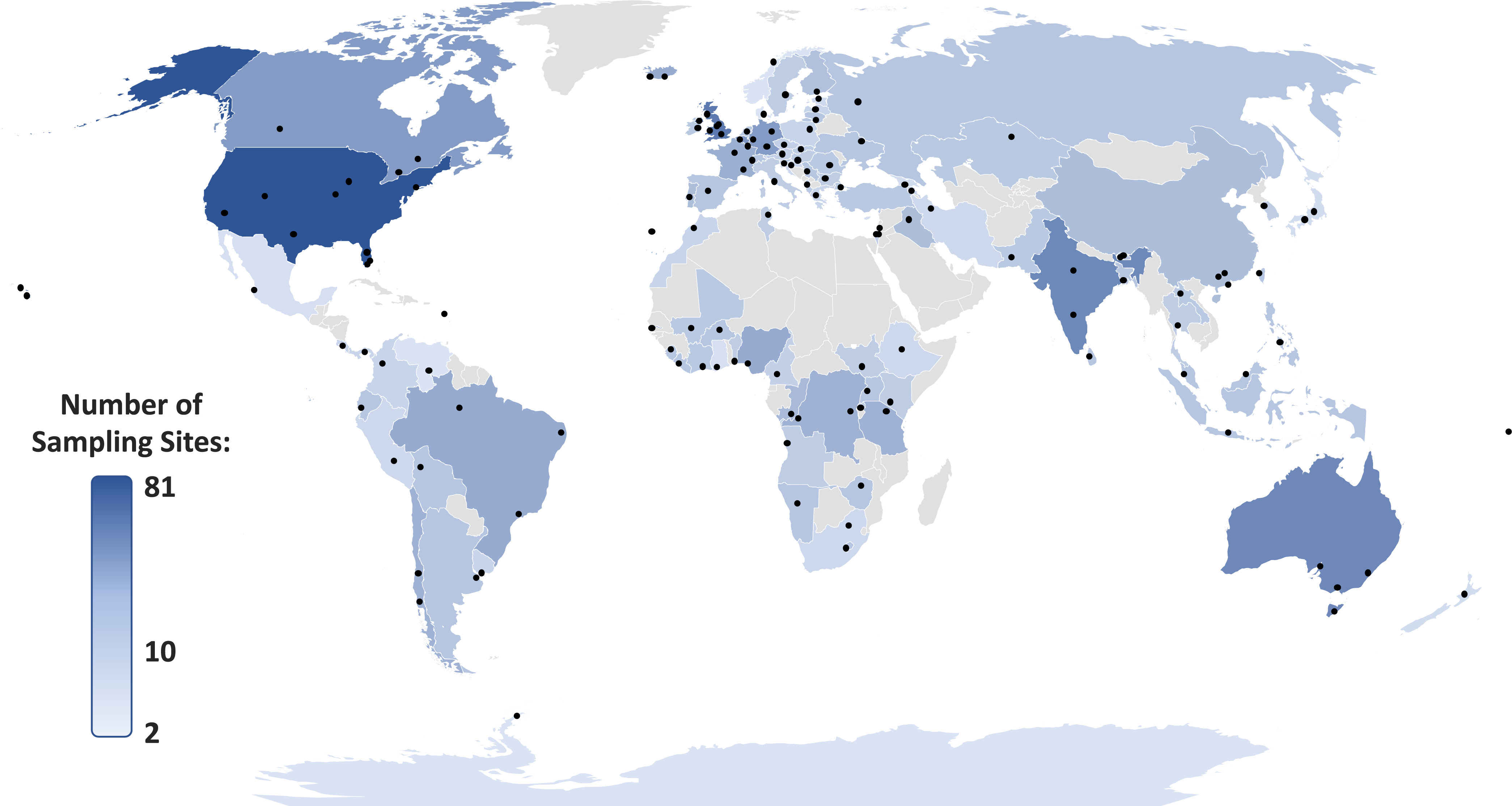
Mappa dei bacini idrografici analizzati nello studio globale (137 in totale). I punti rappresentano gruppi di siti di campionamento distribuiti nei diversi bacini fluviali, mentre i Paesi sono colorati in base al numero totale di campioni raccolti. Fonte: Wilkinson et al, Pharmaceutical pollution of the world’s rivers, PNAS (2022). Licenza: CC BY 4.0
Non tutti i farmaci inquinano allo stesso modo
I farmaci entrano nell’ambiente attraverso diverse vie – dall’escrezione dopo l’uso umano e animale allo smaltimento improprio, fino agli effluenti industriali. Si stima che tra il 30 e il 90% della dose somministrata per via orale sia generalmente escreta come principio attivo nelle urine di animali e umani. «Le classi di farmaci più problematiche sono antidolorifici come ibuprofene e diclofenac, antibiotici come ciprofloxacina e amoxicillina, estrogeni sintetici come l’etinilestradiolo (EE2), antidepressivi, antiepilettici, beta-bloccanti», continua Paolone.
Gli effetti variano anche in base alla destinazione d’uso del farmaco, con differenze importanti tra farmaci umani, veterinari e agrofarmaci. «Le principali differenze tra farmaci umani e veterinari riguardano le vie di rilascio, la concentrazione delle sostanze e le specie ecologiche colpite. I primi tendono a contaminare il suolo attraverso lo spandimento di liquami, mentre i secondi prevalgono nell’inquinamento idrico, costituendo entrambi una minaccia significativa in un contesto di One Health: umana, animale e ambientale», spiega la ricercatrice.
Mentre gli agrofarmaci – pesticidi, erbicidi, fungicidi e insetticidi – destano preoccupazione soprattutto per l’emivita lunga (il tempo necessario affinché concentrazione, attività o quantità di una sostanza si riduca al 50% del valore iniziale), la persistenza nell’ambiente (accumulo per lunghi periodi) e la resistenza al dilavamento (rimozione da parte di pioggia o irrigazione). «Il suolo è il primo recettore. Alcune molecole hanno emivita molto lunga e si accumulano negli strati profondi, alterandone il microbiota. Inoltre attraverso il ruscellamento raggiungono fiumi, laghi e falde acquifere, con conseguente tossicità per pesci, anfibi e invertebrati acquatici. Nel mio laboratorio abbiamo confermato gli effetti neurotossici di alcuni pesticidi in un modello preclinico. Alcune sostanze alterano l’orientamento, la memoria e la riproduzione delle api, così come ne risentono gli uccelli insettivori. Il quadro normativo è complesso e in forte evoluzione. Il pilastro centrale è il Regolamento (CE) n. 1107/2009, che disciplina l’autorizzazione e l’immissione sul mercato dei prodotti fitosanitari. Il sistema funziona su due livelli, l’Autorità europea per la sicurezza alimentare (EFSA) valuta le sostanze attive, mentre gli stati membri valutano e autorizzano i prodotti a livello nazionale. In Italia l’Istituto Superiore per la Protezione e la Ricerca Ambientale (ISPRA) monitora e valuta l’impatto ambientale dei fitofarmaci. I residui negli alimenti sono invece disciplinati dal Regolamento (CE) 396/2005», prosegue Paolone.
La situazione in Italia
In Italia, le analisi delle acque, condotte in 23 stazioni distribuite lungo il territorio e selezionate nei punti più critici (a valle dei depuratori, nelle aree urbane e nei contesti agricoli) mostrano una presenza diffusa di farmaci nell’ambiente, soprattutto di farmaci come il diclofenac e ormoni (estradiolo ed estrone). È quanto emerge dal primo rapporto ISPRA sul monitoraggio delle sostanze della Watch List, un sistema europeo di sorveglianza delle sostanze emergenti previsto dalla Direttiva 2013/39/UE per valutarne i rischi ambientali. In alcuni casi le concentrazioni raggiungono centinaia di nanogrammi per litro (oltre 600 ng/L per il diclofenac e fino a 400 e 200 ng/L rispettivamente per azitromicina e claritromicina) con una marcata stagionalità legata all’aumento delle prescrizioni nei mesi invernali. Il quadro evidenzia una distinzione tra fonti urbane e rurali, ma un’origine comune: l’uso diffuso di farmaci, i cui residui sfuggono ai sistemi di depurazione e raggiungono i corpi idrici.
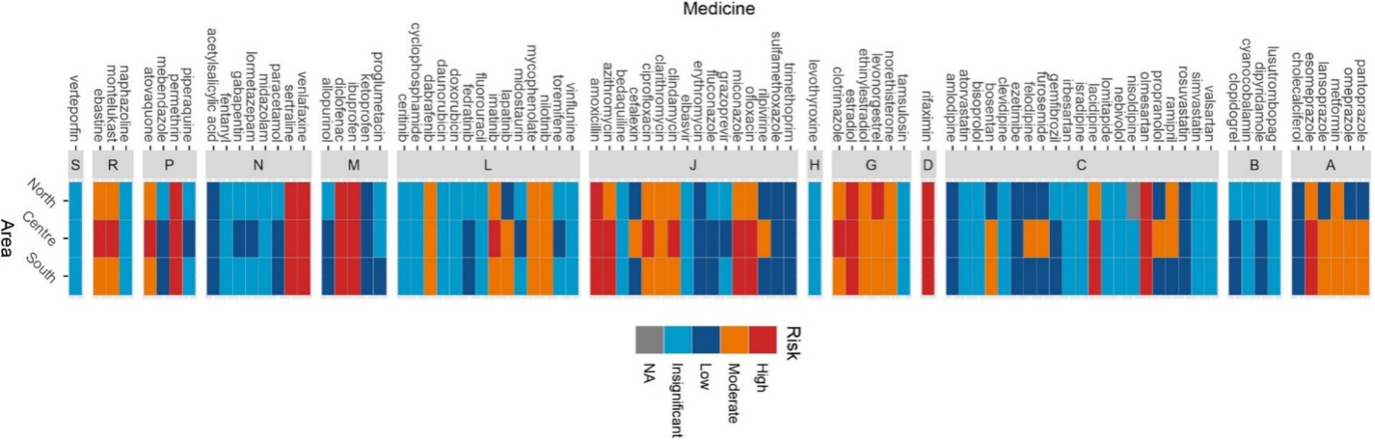
Livello di rischio dei 90 farmaci selezionati nel 2022, suddiviso per macro-area italiana. Le lettere maiuscole indicano i gruppi di livello I dell’ATC. Fonte: Giunchi et al, Assessing the environmental impact of medicines in Italy using data from the Italian Medicines Agency. Bri Cilm Pharmacol (2025) Licenza: CC BY 4.0
In Italia sono stati identificati 13 farmaci ad alto rischio ambientale, tra cui betabloccanti (olmesartan, lacidipina), antibiotici (amoxicillina, azitromicina, ofloxacina), antidepressivi (venlafaxina, sertralina) e antiparassitari (permetrina, atovaquone). Un recente studio dell’Università di Bologna e dell’Agenzia Italiana del Farmaco (AIFA) ha integrato dati provenienti da OsMed, il database dell’AIFA che monitora consumi e prescrizioni di farmaci in Italia, e indicatori di tossicità ecologica, analizzando i farmaci più prescritti, quelli inclusi nelle Watch List europee e le molecole più pericolose per gli ecosistemi acquatici. Quasi la metà dei principi attivi è risultata di interesse tossicologico, per l’elevato utilizzo (come amoxicillina, ibuprofene e diclofenac) o per valori molto bassi di concentrazione predittiva di tossicità (PNEC), la soglia sotto la quale una sostanza non dovrebbe causare danni agli ecosistemi: valori molto bassi segnalano una maggiore criticità ambientale (come nel caso di estradiolo e lacidipina).
Il rischio non è uniforme sul territorio: il Centro emerge come area più critica, con la presenza di numerosi principi attivi ad alto rischio, tra cui clotrimazolo, clindamicina, ciprofloxacina, imatinib, montelukast, ebastina e atovaquone. Centro e Sud mostrano un maggiore consumo di antibiotici, come azitromicina e ofloxacina, e antimicotici come il miconazolo. Nel Nord, invece, prevale l’uso di ormoni a scopo contraccettivo (levonorgestrel).
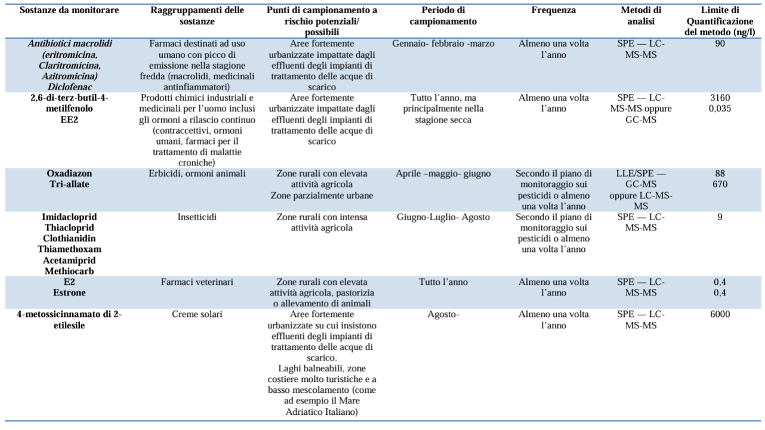 Molecole incluse nella Watch List europea, con indicazione di periodi e modalità di monitoraggio nelle acque superficiali. Fonte: ISPRA, Primo rapporto sul monitoraggio delle sostanze della Watch List.
Molecole incluse nella Watch List europea, con indicazione di periodi e modalità di monitoraggio nelle acque superficiali. Fonte: ISPRA, Primo rapporto sul monitoraggio delle sostanze della Watch List.
Dispositivi e rifiuti: l’impatto nascosto delle terapie GLP-1
Un’altra grande categoria di farmaci che sta facendo discutere per il potenziale contributo all’inquinamento e l’impatto sulla salute degli ecosistemi è quella delle terapie con agonisti del GLP-1, oggi sempre più diffusi nel trattamento di diabete di tipo 2 e obesità. «Si tratta di molecole molto diverse dai farmaci tradizionali», spiega Raffaella Sorrentino, membro del Gruppo di lavoro sull’impatto ambientale dei farmaci della Società Italiana di Farmacologia (SIF). «Sono peptidi, cioè catene di amminoacidi, la cui produzione richiede processi complessi, con un uso intensivo di solventi e numerosi passaggi di purificazione. Ne deriva l’elevato E-factor, cioè la quantità di scarti generati per ogni chilogrammo di prodotto, che rende questi farmaci più “pesanti” in fase produttiva rispetto a molte piccole molecole. Dal punto di vista complessivo, l’impatto ambientale di queste terapie deriva da tre componenti principali: la sintesi del principio attivo, relativamente intensiva in termini di solventi; la produzione dei dispositivi di somministrazione; e la gestione dei rifiuti».
Secondo alcune stime, per produrre un solo chilogrammo di questi farmaci possono servire fino a 14.000 kg di solventi, contro i 300 kg circa necessari per i farmaci tradizionali. A questo si aggiunge l’impatto dei dispositivi: le terapie sono spesso somministrate tramite penne o siringhe pre-riempite, che garantiscono precisione di dosaggio, stabilità del principio attivo e facilità d’uso, ma contribuiscono alla produzione di rifiuti plastici. Tuttavia, osserva Sorrentino, tecnologie analoghe esistono da anni (come per insulina ed eparina) e stanno evolvendo verso soluzioni riutilizzabili e più efficienti, anche per i GLP-1, con lo sviluppo di formulazioni orali.
Inoltre, «I GLP-1 sono attivi a quantità molto basse, dell’ordine di pochi milligrammi (mg), rispetto ad antibiotici o analgesici di largo consumo (dosaggio vicino al grammo). Per esempio, nel trattamento del diabete tipo 2 gli agonisti del GLP-1 sono attivi a 2-5 mg e la somministrazione di solito è settimanale. Mentre le sulfaniluree oscillano tra 5-10mg o 30-120 mg al giorno e sono spesso usati in combinazione con la metformina, con dosaggi medi di 500 mg, 2-3 volte al dì», continua Sorrentino.
Questo consente, a parità di patologia, di trattare molti più pazienti diabetici e nel contempo ottenere benefici clinici notevoli, come la riduzione delle complicanze cardiovascolari e renali e minore ricorso a ulteriori terapie e ospedalizzazioni che a loro volta impatterebbero sull’ambiente.
Dati parziali, problema globale
Se le evidenze su animali ed ecosistemi sono numerose, non vale lo stesso per gli effetti sull’essere umano, specie quelli relativi a un’esposizione cronica, ancora poco chiari. «Inoltre, i metaboliti sono poco monitorati», puntualizza Paolone. «Spesso il farmaco escreto è parzialmente metabolizzato e i metaboliti possono essere più o meno attivi del composto iniziale. Infine, c’è da considerare che molte molecole spesso si ricombinano insieme nell’ambiente».
Mancano depuratori progettati per rimuovere i farmaci e limiti legali per la quasi totalità dei farmaci nell’acqua potabile, insieme a una valutazione esaustiva del rischio ambientale pre-immissione in commercio. A questo si aggiunge la conoscenza fortemente disomogenea a livello globale: «I Paesi a basso e medio reddito sono monitorati pochissimo. Nonostante le concentrazioni di antibiotici rilevate in alcuni fiumi siano di ordini di grandezza superiori a quelli europei ma i dati sistematici mancano», prosegue la ricercatrice.
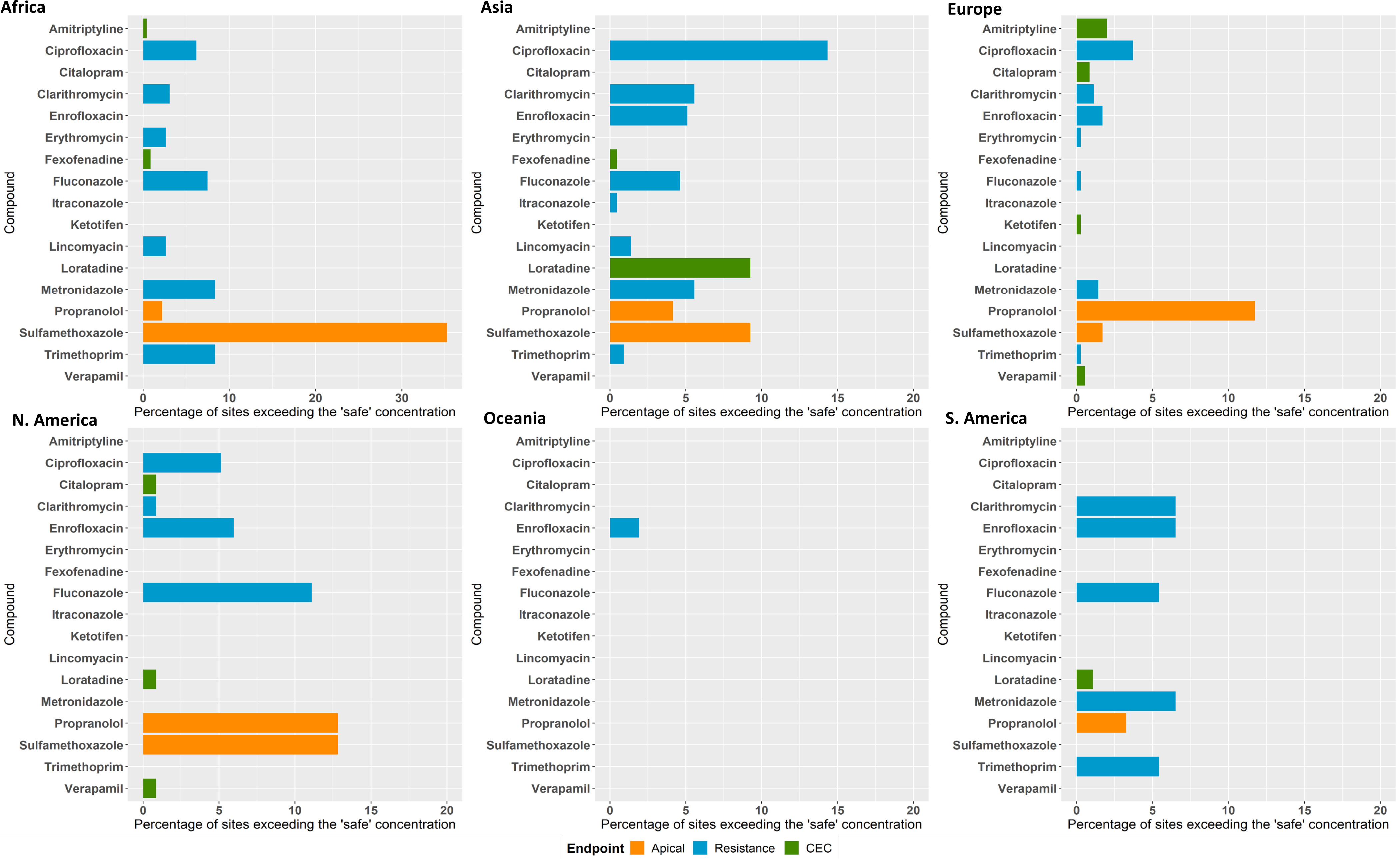 Percentuale di siti del monitoraggio globale in cui le concentrazioni rilevate superano diverse soglie di sicurezza: quelle ecotossicologiche per organismi acquatici (arancione), quelle ambientali critiche (CEC) basate sugli effetti farmacologici stimati (verde) e quelle legate al rischio di resistenze antimicrobiche (blu). Fonte: Wilkinson et al, Pharmaceutical pollution of the world’s rivers, PNAS (2022). Licenza: CC BY 4.0
Percentuale di siti del monitoraggio globale in cui le concentrazioni rilevate superano diverse soglie di sicurezza: quelle ecotossicologiche per organismi acquatici (arancione), quelle ambientali critiche (CEC) basate sugli effetti farmacologici stimati (verde) e quelle legate al rischio di resistenze antimicrobiche (blu). Fonte: Wilkinson et al, Pharmaceutical pollution of the world’s rivers, PNAS (2022). Licenza: CC BY 4.0
Secondo un’ampia revisione della letteratura, condotta dall’Università di York e dal Centro di scienze idriche del Midwest centrale del Servizio Geologico degli Stati Uniti (USGS) e pubblicata nel 2022 su PNAS, la maggior parte delle ricerche si è concentrata su 75 Paesi su 196, in particolare in Nord America ed Europa occidentale. «Il minore spettro di farmaci rilevati in Africa e negli stati dell’America Latina e dei Caraibi non è dovuto a livelli di inquinamento inferiori, ma alla mancanza di laboratori ambientali attrezzati e finanziati per monitorare i farmaci nelle matrici ambientali», spiega Emanuela Testai, membro del Consiglio Direttivo della Società Italiana di Tossicologia (SITOX). «Le apparecchiature necessarie sono costose da acquistare e da mantenere; pertanto, quasi tutti i campioni d’acqua inclusi nel database per l’Africa (con l’eccezione del Sudafrica) sono stati analizzati in paesi industrializzati».
La review condotta dall’USGS ha scoperto che i campioni più contaminati prevenivano proprio dalle zone geografiche sottorappresentate, come Paesi africani (Etiopia, Tunisia, Repubblica Democratica del Congo, Kenya e Nigeria) e asiatici (Pakistan, India, Armenia, Palestina, Cina). Diversi principi attivi farmaceutici (API), come il paracetamolo, sono stati rilevati in tutti i continenti. I valori di carbamazepina, metformina e caffeina superavano il 50%. Circa un quarto dei siti campionati ha riportato valori di API con potenziali effetti ecologici, in particolare per sulfametossazolo, propranololo, loratadina, amitriptilina, citalopram, fexofenadina, verapamil e ketotifene. 9 antibiotici su 13 superavano le soglie di sicurezza, con la ciprofloxacina che ha superato il limite in 64 siti.
Effetto cocktail: quando gli inquinanti si incontrano
Quando si parla di sostanze persistenti nell’ambiente, il pensiero corre anche verso un’altra grande famiglia di molecole, quella delle sostanze per- e polifluoroalchiliche (PFAS), utilizzate per le loro proprietà di resistenza all’acqua, al grasso e alle macchie in numerosi prodotti. «PFAS, farmaci attivi e microplastiche spesso coesistono nei comparti acquatici a causa di scarichi urbani e non, acque reflue e altre fonti antropiche», spiega Testai. «Oggi non ci sono evidenze sperimentali sufficientemente robuste che dimostrino gli impatti a lungo termine associati alla presenza contemporanea di queste sostanze negli ecosistemi naturali».
Ma se la triade API-microplastiche-PFAS è improbabile, caso ben diverso è quello dell’interazione tra microplastiche e PFAS, dove le prove a supporto sono in aumento: «Le prime possono fungere da vettori per alcuni PFAS, che si adsorbono (ovvero aderiscono) sulla loro superficie per le loro proprietà chimico-fisiche, con implicazioni per la tossicità complessiva nell’ambiente. È meno plausibile che ciò possa accadere con principi attivi di farmaci, generalmente con forti caratteristiche di idrosolubilità», continua la ricercatrice.
Le microplastiche non vengono “assorbite” nel tratto gastrointestinale, essendo eliminate con le feci. Tuttavia, il passaggio nell’apparato intestinale può favorire processi infiammatori, perché le sostanze sulla loro superficie possono essere rilasciate e diventare biodisponibili – essere cioè assorbite dai tessuti ed entrare nel circolo sanguigno. «Oggi una parte della ricerca si concentra proprio sulle esposizioni combinate di più sostanze, con approcci sempre più raffinati, come quelli promossi dall’EFSA. La valutazione dei rischi avviene di solito in ottica One Health, in modo da avere un quadro completo. Per esempio, da decenni le richieste di produzione di dati regolatori coprono i tre pilastri One Health (umano, animale e ambiente) per valutare la sicurezza di pesticidi e biocidi».
Tra innovazione tecnologica e vuoti normativi
Una prima risposta viene dalla Direttiva UE 2024/3019, recentemente entrata in vigore e al centro di forti tensioni con l’industria farmaceutica, perché rafforza gli obblighi su raccolta e trattamento delle acque reflue urbane. Ma il vero salto di qualità, secondo Testai, «Sarebbe combinare la riduzione del consumo di farmaci con il potenziamento degli impianti di depurazione, tecnologie avanzate e pensate per le caratteristiche chimico fisiche dei principi attivi dei farmaci e/o dei metaboliti (spesso diverse dalle sostanze chimiche considerate tradizionalmente come ‘inquinanti’)».
Soluzioni efficaci su cui hanno investito in Europa Paesi come Germania, Paesi Bassi e Svezia, ma costose e difficili da implementare su larga scala. Anche i progressi avvenuti nel campo delle biotecnologie e la digital transformation, che hanno rivoluzionato la medicina e il modo di progettare i farmaci, potrebbero rivelarsi preziosi. «Lo sviluppo di farmaci biologici e terapie geniche ad alta selettività ha aumentato l’efficacia dei trattamenti e ne ha ridotto gli effetti collaterali, insieme all’uso di nanotecnologie, che consentono di ingegnerizzare nanoparticelle capaci di veicolare i principi attivi direttamente nelle cellule bersaglio», continua Testai. L’avvento dell’industria 4.0 (la convergenza tra sistemi fisici e tecnologie digitali come la stampa3D e i Big data) ha reso possibile la medicina di precisione e l’utilizzo quantità di farmaco esatta, evitando sovradosaggi. L’Intelligenza artificiale (AI) e il machine learning potrebbero supportare la progettazione di nuove molecole anche da zero, riducendo tempi e costi della ricerca.
Restano però dei limiti, fa notare Testai: «Queste tecnologie sono applicabili solo a principi attivi noti e la loro produzione è energivora e complessa (bioreattori, purificazione, catena del freddo), richiedono spesso refrigerazione, possono generare molti rifiuti (materiali monouso sterili, plastica, filtri) e il destino ambientale delle molecole utilizzate è quasi sempre sconosciuto».
Curare senza inquinare: la sfida della medicina sostenibile
A questo punto la domanda non è più se i farmaci abbiano un impatto sull’ambiente, ma come ridurlo senza compromettere i benefici per la salute. Una delle risposte più promettenti è la progettazione “green”, «Che mira a integrare sostenibilità ambientale e salute umana già nella fase di ideazione e sviluppo delle molecole e dei processi produttivi», racconta Testai. «Ciò significa progettare molecole meno persistenti, adottare principi di chimica verde nei processi di sintesi e formulazione, processi produttivi sostenibili ed efficienti, limitando l’uso di sostanze tossiche e la produzione di scarti. Questi criteri rientrano nel paradigma del Safe and Sustainable by Design (SSbD), un approccio che mira a ridurre effetti indesiderati sia per i pazienti sia per gli ecosistemi fin dalla progettazione».
Il quadro normativo rimane però controverso. Per esempio, nell’Unione europea il regolamento CLP (Classification, Labelling and Packaging), molto conservativo, si limita alla valutazione della pericolosità di una sostanza indipendentemente dalla dose di esposizione, che è invece un pilastro fondamentale quando si esamina il profilo di sicurezza di qualunque sostanza chimica. Poi c’è il problema degli interferenti endocrini, «Sostanze che possono alterare il funzionamento del sistema endocrino umano causando disfunzioni ormonali, già soggetti alle severe restrizioni imposte dal regolamento REACH (Registration, Evaluation, Authorization of CHemiclas) adottato dal Parlamento Europeo, sebbene manchino ancora criteri condivisi a livello internazionale», spiega Paolone.
Ma accanto ai limiti, stanno emergendo nuovi modelli di governance: «Tra le proposte più discusse c’è il principio di responsabilità estesa del produttore, secondo cui chi immette un farmaco sul mercato dovrebbe contribuire ai costi del suo trattamento nelle acque reflue. In Europa, la Francia ha introdotto meccanismi simili», continua la ricercatrice.
La direzione è chiara, ma l’integrazione tra sostenibilità, innovazione e pratica clinica deve ancora avvenire. È il concetto di appropriatezza ambientale, che rappresenta l’estensione naturale di due pilastri della pratica clinica: appropriatezza prescrittiva e aderenza alla terapia. «Significa usare il farmaco giusto, per il paziente giusto, nel momento giusto e per il tempo necessario, migliorando esiti clinici, riducendo sprechi e trattamenti inutili e, di conseguenza, abbassando anche l’impatto ambientale complessivo», conclude Sorrentino.